Adempas® feiert Geburtstag
-
 ©Bayer Vital GmbH
©Bayer Vital GmbH -
 ©Bayer Vital GmbH
©Bayer Vital GmbH -
 ©Bayer Vital GmbH
©Bayer Vital GmbH -
 ©Bayer Vital GmbH
©Bayer Vital GmbH
Pulmonale Hypertonie (PH)
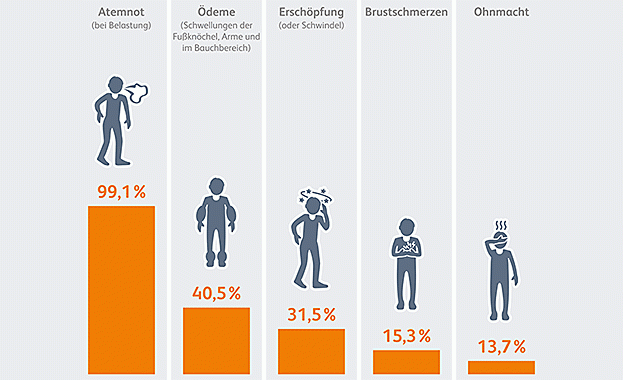
Je nach Ursache der Entstehung sind mehrere Formen der PH bekannt, so die CTEPH und die PAH. Die genauen Ursachen der Entstehung der CTEPH, der chronisch thrombembolischen pulmonalen Hypertonie sind bislang nicht bekannt. Es wird jedoch davon ausgegangen, dass eine vorausgegangene Lungenembolie nach tiefer Beinvenenthrombose dazu beitragen kann oder, in Fällen in denen keine Lungenembolie vorlag, in den Lungengefäßen selbst bindegewebige Veränderungen stattfinden, die den Blutfluss behindern und zur Hypertonie führen. Die Patienten klagen über Atemnot, Müdigkeit, Schwäche in den unteren Extremitäten, dumpfe Brustschmerzen, Schwindelanfälle oder auch Bewusstlosigkeit. In fortgeschrittenem Stadium kommt es zu Wasseransammlungen im Gewebe und zu Gewichtzunahme. Da diese Beschwerden ziemlich unspezifisch sind, die CTEPH außerdem eine recht seltene Erkrankung, dauert es oft bis zu 2 Jahren, bis die richtige Diagnose gestellt wird. Behandelt wird die CTEPH durch eine pulmonale Endarterektomie, der Ausschälung der Lungenarterien, womit die Erkrankung geheilt werden kann.
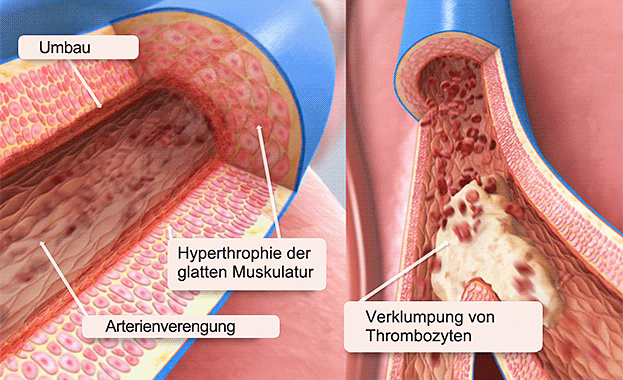
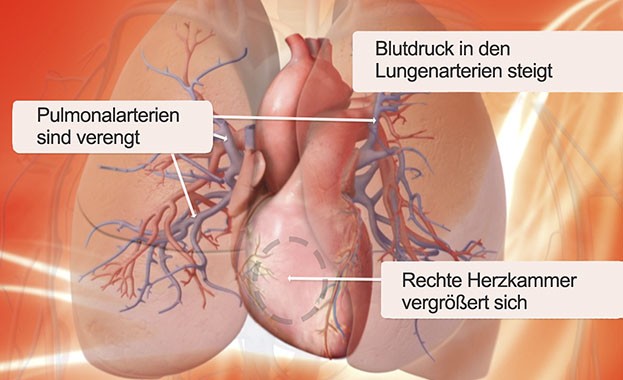
Bei der PAH, der pulmonalen arteriellen Hypertonie sind die Gefäße aus bislang unbekannten Ursachen stark verengt und es kommt zu einem erhöhten Druck in den Lungenarterien. Das rechte Herz muss gegen diesen Widerstand pumpen und erheblich mehr leisten, was letztlich zu seiner Schwächung führen kann. Durch die verengten Gefäße ist die Sauerstoffabgabe ins Blut und somit die Sauerstoffversorgung der Organe erschwert. Dieser Sauerstoffmangel und die zunehmende Schwäche der rechten Herzhälfte sind für die Symptome der PAH wie Atemnot oder rasche Erschöpfbarkeit verantwortlich. Die PAH wird medikamentös behandelt; wenn diese Behandlung versagt, muss eine Lungentransplantation in Erwägung gezogen werden.
Vor genau einem Jahr wurde Adempas® (Riociguat, Bayer Vital GmbH) zur Behandlung zweier Formen des Lungenhochdrucks – CTEPH und PAH – zugelassen. Riociguat ist ein Stimulator des Enzyms lösliche Guanylatcyclase (sGC), welches der einzige bekannte Rezeptor von Stickstoffmonoxid (NO), einer körpereigenen gefäßerweiternden Substanz, ist. NO aktiviert die sGC und sorgt über einen weiteren Botenstoff dafür, dass die glatten Muskelzellen der Gefäßwände entspannen, wodurch in der Lunge der Blutdruck gesenkt und das Herz entlastet wird. Ist zu wenig NO vorhanden, kann sGC nicht aktiviert werden. Hier greift nun Adempas® ein: es sensibilisiert die sGC für das im Körper der Patienten noch vorhandene NO. Gleichzeitig stimuliert es sGC direkt, auch in Abwesenheit von NO, was besonders wichtig ist, weil bei der pulmonalen Hypertonie ein NO Mangel besteht. Die Wirksamkeit und Verträglich von Adempas® wurde bereits vor der Zulassung in großangelegten klinischen Studien untersucht. Nächstes Ziel nach der Zulassung war die Erfassung der Langzeitwirkung und Langzeitverträglichkeit in den beiden Indikationen CTEPH und PAH.
In die CHEST-2 Studie, eine Fortsetzung der CHEST-1 Studie, wurden Patienten mit inoperabler oder persistierender und chronischer CTEHP eingeschlossen. Endpunkte nach einjähriger Behandlung waren die 6-Minuten-Gehstrecke (6MWD), die WHO-Funktionsklasse und die Häufigkeit von Nebenwirkungen. Die 6MWD verbesserte sich um +59 m gegenüber dem Ausgangswert, ebenso verbesserte bzw. stabilisierte sich die WHO Funktionsklasse bei 50% bzw. 45% der Patienten. Ihre Lebensqualität nahm zu: „In der Praxis bedeutet die Verlängerung der Gehstrecke für Patienten einen enormen Fortschritt, denn sie können ihren Alltag wieder besser bewältigen“ kommentiert Prof. Dr. med. Stephan Rosenkranz, Köln. „Insgesamt wurde Adempas® gut vertragen“, resümiert er weiter, obwohl 90% der Patienten die maximale Dosis von 3x2,5 mg täglich erhalten hatten.
Ein vergleichbar positives Bild – Verlängerung der 6-Minunten-Gehstrecke, die auch im weiteren Verlauf beibehalten werden konnte, Verbesserung der WHO Funktionsklasse und nur wenig Nebenwirkungen ergibt sich auch bei den PAH-Patienten, die in den PATENT Studien (PATENT 1 und 2) untersucht wurden.
Adempas® ist das erste zugelassene Medikament für inoperable oder postoperativ persistierende oder rezidivierende Patienten mit CTEPH. Zwar bleibt die pulmonale Endarterektomie das Verfahren der Wahl, da die Erkrankung dadurch geheilt werden kann. Aber bis zu 40% der Patienten kommen für den Eingriff nicht in Frage und bis zu 35% müssen damit rechnen, dass auch nach der Operation der Lungenhochdruck weiter bestehen bleibt oder sogar rezidiviert. Nicht nur bei diesen Patienten hat Adempas® seinen therapeutischen Nutzen im klinischen Alltag unter Beweis gestellt. „Auch PAH Patienten profitieren davon, weil es sich als wertvolle Therapieergänzung zu der bestehenden Behandlung gezeigt hat“, betont Rosenkranz. Adempas® (Riociguat) wird weiter untersucht, um neue Indikationen zu erschließen. Seit 2014 arbeitet Bayer Vital GmbH in Kooperation mit Merck & Co an der Weiterentwicklung nicht nur von Riociguat sondern auch an der Substanzklasse der sGC Stimulatoren, um deren Potential in der Behandlung der pulmonalen Hypertonie und weiterer Erkrankungen zu erforschen.
