Bakteriophagen: Bakterienfressende Viren
-
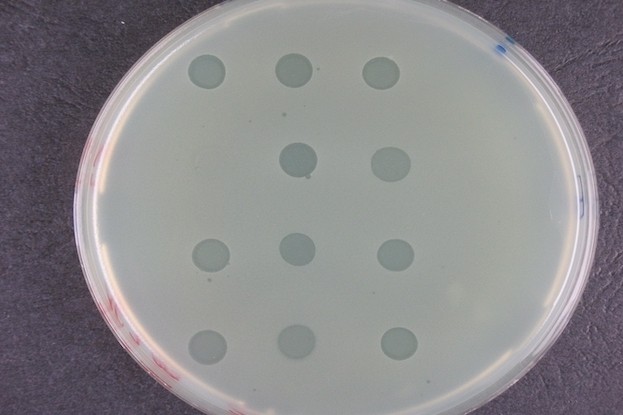
![Bakterienrasen mit Löchern, die durch Phagen verursacht werden - ©Leibniz-Institut DSMZ Bakterienrasen mit Löchern, die durch Phagen verursacht werden]() Bakterienrasen mit Löchern, die durch Phagen verursacht werden - ©Leibniz-Institut DSMZ
Bakterienrasen mit Löchern, die durch Phagen verursacht werden - ©Leibniz-Institut DSMZ
Bakteriophagen, abgekürzt meist nur als Phagen bezeichnet, sind in ihrem Nutzungspotenzial für die Medizin erst bekannt, seit die Antibiotikaresistenzen als Stichwort immer häufiger auftraten. Phagen (aus dem Griechischen: Bakterienfresser) sind die häufigste Daseinsform auf unserem Planeten. Es handelt sich dabei um Viren, die Bakterien spezifisch zerstören können. Im globalen Surveillance Report der WHO wird das erschreckende Ausmaß der Verbreitung multiresistenter Bakterien (Antimikrobielle Resistenz = AMR) verdeutlicht. Auch sie können, wie es die derzeit grassierende Corona-Pandemie mehr als deutlich zeigt, wachsende AMR-bedingte Sterblichkeitsraten, eine Kostenexplosion im Gesundheitssystem sowie Umweltschädigungen durch Einbringung von AMR in die Tiermast von globaler Tragweite nach sich ziehen.
Dr. Christine Rohde vom Leibniz-Institut DSMZ erklärt dazu: “Die AMR-Forschung adressiert neben der Suche nach neuen Antibiotika auch Bakteriophagen als Ergänzung oder Ersatz von Antibiotika. Phagen werden im Gegensatz zu den „statischen Drogen/Substanzen“ auch „intelligente Antibiotika“ genannt. Sie sind die natürlichen Gegenspieler der Bakterien und können da eingesetzt werden, wo Bakterien unerwünscht sind, also als Antiinfektiva in der Medizin. Phagen vermehren sich am Infektionsort, solange ihre passenden Beutebakterien vorhanden sind und zerfallen danach wieder in ihre Bausteine (Protein und Nukleinsäure). Damit sind sie selbst-regulierende Antiinfektiva, die zudem spezifisch wirken”. Ein Phage kann spezifisch nur Bakterien einer Art erkennen und zerstören. Wir Menschen tragen eine Unmenge an Phagen in unserem Mikrobiom… Erkrankt man an einer bakteriellen Infektion und wendet Phagen anstelle von Antibiotika an, verschiebt man im Grunde in der Erkrankung nur das Gleichgewicht zugunsten der passenden Phagen, um den Überschuss der pathogenen Bakterien zu eliminieren. Phagen haben demzufolge ein großes Potenzial… und können gegen fast alle Bakterien mit Ausnahme derer, die einen intrazellulären Lebenszyklus haben, eingesetzt werden. Dazu gehören beispielsweise die Erreger der Borreliose oder der Tuberkulose.
Phagencocktail gegen Mukoviszidose
Am Leibniz-Institut DSMZ startete 2017 mit Phage4Cure ein erstes deutsches Projekt mit dem Ziel einer klinischen Studie, in der ein hochaufgereinigter Phagencocktail inhalativ bei Patienten mit Bronchiektasen und Mukoviszidose eingesetzt werden soll.
In diesem Pilotprojekt zeigt sich auch die Komplexität einer klinischen Studie mit arzneimittelrechtlicher Herstellung: Phagen als API (aktiver pharmazeutischer Inhaltsstoff) und dem Zulassungsprozess durch BfArM (Bundesinstitut für Arzneimittel und Medizinprodukte), mit präklinischem Teil und schließlich der Erprobung an gesunden Probanden.
Ein weiteres Forschungsprojekt nennt sich PhagoFlow und hier sollen größere Zahlen verschiedener Phagen für Patienten mit “Wunden der unteren Extremität” in magistraler Anwendung verfügbar werden.
Es bleibt spannend, denn zweifelsohne gehört die Phagenforschung zu einer der Säulen, die zur Bekämpfung der Antibiotikarestistenzen dringendst benötigt werden.
Schlagwörter
Phagen
Phagentherapie
Antibiotika
Mukoviszidose