Cystische Fibrose: chronische Infektionen mit Lungenkeim verhindern
-
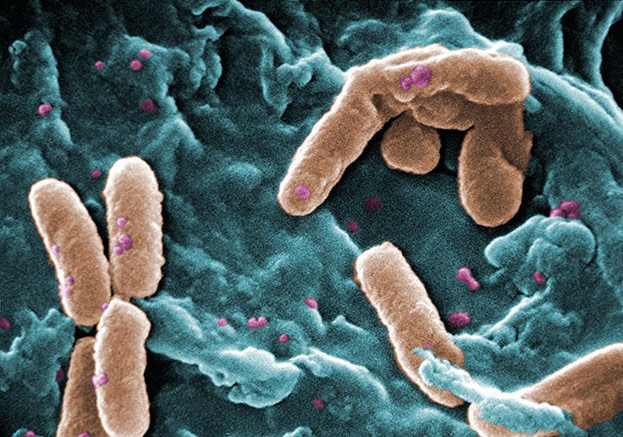 Pseudomonas aeruginosa - ©Janice Haney Carr
Pseudomonas aeruginosa - ©Janice Haney Carr
Entgegen früherer Annahmen sind auch die Atemwege inklusive der Lunge nicht steril, sondern vergleichbar mit dem Darm eine ökologische Nische für eine Vielzahl von Mikroorganismen, die zum Teil noch unbekannt sind. Ist diese Lebensgemeinschaft – das Mikrobiom – im Gleichgewicht, geht es dem Menschen gut, nehmen bestimmte schädliche Keime überhand, kann es zu Lungenentzündungen und Einschränkungen der Atemfunktion kommen. Doch was ist zuerst da – ein gestörtes Mikrobiom, das Krankheitserregern Tür und Tor öffnet? Oder führt erst eine chronische Infektion mit bestimmten Bakterien dazu, dass eine normale Lebensgemeinschaft verdrängt wird? Prof. Dr. Alexander Dalpke, Stellvertretender Ärztlicher Direktor der Abteilung Medizinische Mikrobiologie und Hygiene, und Prof. Dr. Marcus A. Mall, Leiter des Mukoviszidose-Zentrums des Universitätsklinikums Heidelberg, gelang es nun, für Patienten mit Cystischer Fibrose diese wichtige Frage zu klären. „Unsere Befunde zeigen, dass Mikrobiom-Veränderungen die Folge, nicht aber die Ursache einer Infektion mit dem Bakterium Pseudomonas aeruginosa sind“, sagt Prof. Dr. Alexander Dalpke.
Die Forscher analysierten dafür wiederholt gewonnene Proben, in denen dann erstmalig oder regelmäßig das Bakterium Pseudomonas aeruginosa nachgewiesen wurde. Die Ergebnisse der aktuellen Studie, die vom Deutschen Zentrum für Lungenforschung unterstützt wurde, erschienen aktuell in der Fachzeitschrift „European Respiratory Journal“.
Mikrobiom-Untersuchungen durch Genom-Sequenzierung
Bei Patienten mit der erblichen Multiorganerkrankung Cystische Fibrose (Mukoviszidose) ist der Schleim in den Bronchien zähflüssiger als bei gesunden Menschen. Das zähe Sekret kann vom Flimmerepithel nur schwer abtransportiert werden und stellt deshalb ein Nährmedium für verschiedene Mikroorganismen dar, zu denen auch das bei der Cystischen Fibrose gefürchtete Bakterium Pseudomonas aeruginosa gehört, welches bei den Betroffenen zu einem schnelleren Verlust der Lungenfunktion führt. Klassischerweise werden Pseudomonas-Infektionen über Zellkulturen nachgewiesen. Die Heidelberger Wissenschaftler nutzten jetzt ein Verfahren, mit dem sie Proben der Patienten molekularbiologisch untersuchen und die Mikrobiom-Zusammensetzung aufgrund von Gensequenzen feststellen können. Auf diese Weise war es möglich, Mikrobiom-Veränderungen in Patienten die chronisch, nur phasenweise oder noch gar nicht mit einer Pseudomonas-Infektion zu kämpfen haben, zu untersuchen.
„Bei Erstinfektionen könnte sich eine aggressive Therapie mit Antibiotika lohnen, um die Patienten nicht nur vor einer chronischen Infektion mit Pseudomonas zu schützen, sondern auch um weitere Mikrobiom-Veränderungen zu vermeiden“, so Dalpke. Chronische Pseudomonas-Infektionen können mit Antibiotika nur noch unterdrückt werden, weil die Bakterien dazu neigen, sich zu adaptieren und sich in einem schützenden Biofilm zu verstecken. „Von Cystischer Fibrose betroffene Kinder bleiben bei frühzeitiger Bekämpfung einer Infektion länger Pseudomonas-frei und dies geht nach unseren Untersuchungen mit geringeren Veränderungen des Lungenmikrobioms einher“, fasst der Mikrobiologe Prof. Dr. Alexander Dalpke zusammen.
Über 100 Arten können die Lunge besiedeln – welche Rolle spielen sie?
Insgesamt wurden 392 Proben aus den Atemwegen von 71 Patienten untersucht – darunter dank enger Kooperation mit der Kinderpneumologie des Universitätsklinikums Heidelberg auch Kleinkinder, von denen es bislang wenige Daten gab. Es zeigte sich, dass das Mikrobiom der Lunge aus über 100 verschiedenen, von Patient zu Patient sehr unterschiedlichen Spezies bestehen kann. Unklar ist, ob diese Mikroorganismen, die im Laufe des Lebens aus den oberen Atemwegen die Lunge besiedeln, möglicherweise auch einen schützenden Effekt haben. Prof. Dr. Alexander Dalpke: „Möglicherweise sind Mikroorganismen dieser Gruppe, zu denen zum Beispiel Bakterien der Gattungen Neisseria, Veillonella und Prevotella gehören, sogar mit besseren Lungenfunktionen assoziiert. Dies wird zurzeit kontrovers diskutiert und wird Thema weiterer Forschungsarbeiten sein.“
Schlagwörter
Lunge
Mukoviszidose
Weitere Links zum Thema
Deutsche Zentrum für Lungenforschung (DZL e.V.)
DZL e.V. - 06.10.2017
ist ein vom BMBF und den Ländern geförderter nationaler Verbund, der über 230 Experten auf dem Gebiet der Lungenforschung vereint. Atemwegserkrankungen gehören in Deutschland und weltweit zu den schwerwiegendsten Gesundheitsproblemen und den häufigsten Todesursachen. Der Forschungsverbund verfolgt daher das Ziel durch innovative Forschungsansätze, die Prävention, Diagnose und Therapie von Lungenerkrankungen zu verbessern und Ergebnisse schnell in die Anwendung zu bringen. Die fünf Standortverbünde des DZL sind Borstel/ Lübeck/ Kiel/ Großhansdorf (ARCN), Gießen/ Marburg/ Bad Nauheim (UGMLC), Hannover (BREATH), Heidelberg (TLRC) und München (CPC-M).
Zentrum für Translationale Lungenforschung Heidelberg (TLRC)
TLRC - 06.10.2017
ist ein Standort des Deutschen Zentrums für Lungenforschung (DZL). Ein Schwerpunkt der wissenschaftlichen Arbeiten des interdisziplinären Zentrums für translationale Lungenforschung liegt auf der Aufklärung der den Lungenkrankheiten zugrunde liegenden Prozesse, wie zum Beispiel die chronische Atemwegsentzündung, Schleimüberproduktion, strukturelle Schädigung des Lungengewebes sowie bösartige und andere Neubildungen von Lungengewebe. Das Ziel ist die Verbesserung der Diagnostik und Therapie von chronischen Lungenerkrankungen im Kindes- und Erwachsenenalter durch einen engen Austausch zwischen Grundlagenforschung und klinischer Forschung.
